|
FyzWeb články |
||||
ZÁMĚR ÚLOHYPomocí této úlohy mohou žáci prozkoumat galvanické poměďování. Učitel může podle situace zůstat jen u kvalitativního popisu, nebo zařadit v různé míře i měření a výpočty.
POMŮCKY
TEORETICKÝ ÚVODModrá skalice je pentahydrát síranu měďnatého. Tvoří modré krystaly a je toxická. Při elektrolýze se ve vodném roztoku modré skalice z měďnatých kationtů stávají atomy mědi, které se vylučují na elektrodě. Měříme-li elektrický proud v průběhu elektrolýzy, můžeme odhadnout celkový počet atomů mědi, které se na elektrodě vyloučily.
ÚKOLY
A. PřípravaB. MěřeníC. Úvahy a výpočty
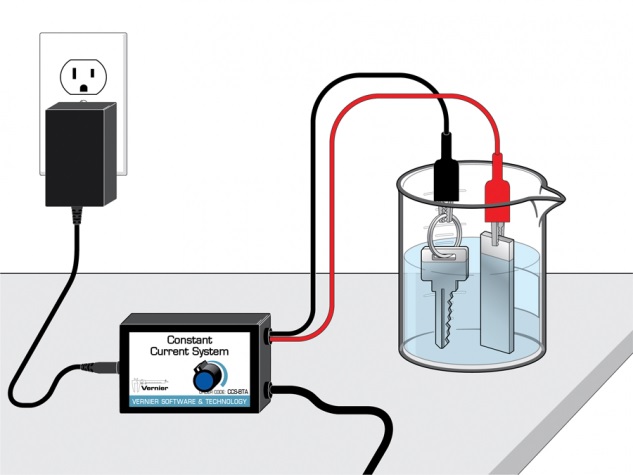
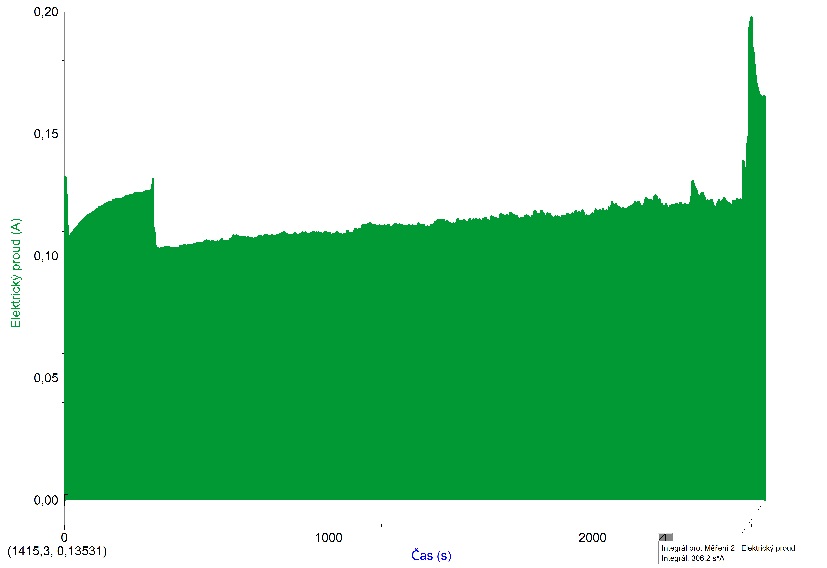
POZNÁMKY PRO UČITELEToxicita modré skalicePozor na to, že modrá skalice je toxická. Baterie LabQuestuLabQuest vydrží v provozu několik hodin. Pokud není na začátku experimentu zcela nabitý nebo pokud chcete provádět experiment velmi dlouho, doporučujeme pro jistotu LabQuest připojit ke zdroji elektrického proudu. ElektrodyIdeální je použít jednu měděnou a jednu uhlíkovou elektrodu. Lze ovšem používat i různé jiné kombinace, můžete poměďovat také třeba klíče nebo hřebíky. Ověřili jsme, že lze použít i obyčejné tuhy do mikrotužky, jak je vidět na videu. Nevýhodou tuhy do mikrotužky je, že se patrně nejedná o čistý uhlík, může pak docházet k rozpouštění nejrůznějších přidaných látek do roztoku. Manipulace s elektrodamiZejména při použití tuh do mikrotužky je třeba počítat s tím, že jsou velmi křehké. Při manipulaci dejte pozor, aby se nezlomily a aby neodpadávala měď, která se na elektrodách vyloučila. K úkolu č. 13Na kladné elektrodě se tvoří bublinky kyslíku. Na záporné elektrodě se vylučuje měď. Vrstva mědi postupně sílí a připomíná barvou i strukturou rez. K úkolu č. 14Z měďnatého kationtu stane atom mědi po přijetí dvou elektronů. K úkolu č. 15Jeden ampér odpovídá toku náboje 1 coulomb za sekundu. Jeden coulomb je 1/(1,602·10-19) elektronů. Půl ampéru za tři sekundy tedy odpovídá množství 9,36 ∙ 1018 elektronů. K úkolu č. 16Při konstantní velikosti elektrického proudu by byl celkový náboj, který prošel elektrodami, roven součinu elektrického proudu a času. V obecném případě odpovídá velikost náboje ploše pod grafem. Pro výpočet plochy pod grafem (numerickou integraci) můžeme využít nástroj Analýza → Integrál. Výsledek je v ampérsekundách, což jsou coulomby. Senzor CCS-BTA během experimentu udržuje proud víceméně konstantní, nicméně k malým změnám docházet může, ať už vlivem změněné velikosti povrchu elektrod, nebo tím, že s elektrodami během experimentu nechtěně pohneme. Při jednom z našich měření (graf níže), které trvalo cca 2500 sekund byl celkový náboj 306,2 ampérsekund (coulombů). Tomu odpovídá 1,94 ∙ 1021 elektronů.
K úkolu č. 17Podle tabulek je relativní atomová hmotnost atomu mědi 63,546, hmotnost jednoho atomu je tedy 1,05 ∙ 10-25 kg. Na každé dva elektrony byl vyloučen jeden atom mědi, dle výsledků úkolu 16 a měření elektrického proudu během elektrolýzy by tedy nárůst hmotnosti poměděné elektrody měl být 0,1008 g. K úkolu č. 18V našem případě měla elektroda na počátku hmotnost 0,22 g, na konci 0,33 g. Rozdíl tedy činí 0,11 g. To je ve vynikající shodě s teoretickým odhadem v úkolu 17.
Materiál vznikl v rámci projektu Gymnázia Cheb s názvem Příprava na Turnaj mladých fyziků. Dostupné ze Školského portálu Karlovarského kraje www.kvkskoly.cz. Autorský tým: Pavel Böhm, Hana Böhmová, Filip Danko, Lucie Filipenská, Petr Kácovský, Věra Koudelková, Daniel Novopacký, Ilona Šimánková, Martin Vlach. Děkujeme i všem ostatním lidem, kteří přispěli k tvorbě materiálů. Pro případ dalších námětů, komentářů, nalezených chyb a podobně využijte e-mailovou adresu pavel.bohm@mff.cuni.cz | ||||